Локальная стероидная терапия остеоартроза с использованием АРТРОФООНА
24.08.2014 в 16:21
Н.А. Хитров
Медицинский Центр Управления Делами Президента Российской Федерации, Москва
Актуальность
Остеоартроз (ОА) – гетерогенная группа заболеваний различной этиологии со сходными биологически-ми, морфологическими, клиническими проявлениями и исходом, в основе которых лежит поражение всех компонентов сустава, в первую очередь хряща, а также субхондральной кости, синовиальной оболочки, связок,капсулы околосуставных мышц. Вторичные воспалительные процессы и, прежде всего синовит, сопровождают течение ОА, формируют клинику болезни и усиливают деструкцию суставных структур [5,6]. Борьба с воспалительным компонентом ОА является одной из ключевых звеньев терапии.На сегодняшний день терапия ОА до конца не разработана и, к сожалению, радикальным пособием остаётся эндопротезирование сустава. Искусство врача состоит в создании условий, когда усиливаются целебные свойс-тва медикамента и нивелируются его побочные действия.Так как пусковым механизмом, эпицентром и конечным инвалидизирующим субстратом при ОА является сустав,то локальная терапия (ЛТ) становится патогенетически обоснованной, клинически значимой и психологически привлекательной, потому, что притягивает внимание больного к конкретному местному лечению, укрепляя сотрудничество врача и пациента в борьбе с недугом.
Положительными особенностями ЛТ являются следующие.
1. Непосредственное воздействие на основной очаг поражения – орган-«мишень», каким при ОА являетсясустав.
2. Достижение оптимальной лечебной концентрации лекарственного препарата в пораженном органе, что уменьшает потребность в системно назначаемых фармакологических средствах. При этом снижается токсическое действие медикаментозных препаратов на организм.
3. ЛТ – важное звено реабилитации ОА, так как проводится лечение именно тех суставов, нарушение функциикоторых является причиной потери трудоспособности.
4. Вовлечённые в патологический процесс различные суставы обладают только им определенной функциональной нагрузкой и в зависимости от этого по-разному определяют прогноз болезни. ЛТ, воздействуя на конкретные суставы, может значительно влиять на качество жизни.
Локальная стероидная терапия (ЛСТ), оказывает симптом-модифицирующие эффекты: обезболивающий,противовоспалительный, улучшающий функции сустава[10,12,14]. Но данные результаты ЛСТ при ОА являются недлительными – 2–3 недели, на что указывают многие авторы и, учитывая возможные отрицательные воздействия стероидов на структуры сустава, ЛСТ показана, на современный момент, не более 2-х раз в год [11,13,15,16]. Преимущественно женский пол, пожилой возраст,частая патология желудочно-кишечного тракта затрудняют общее лечение, особенно применение нестероидных противовоспалительных препаратов (НПВП)у больных ОА. Многообразие форм и высокая частота сопутствующей соматической патологии при ОА также диктуют правильное сочетание ЛТ со средствами об-щего воздействия [2].Проблема состоит в том, что широко используемая ЛСТ и НПВП имеют много общих побочных действий на организм человека, одинаково негативно воз-действуют на хрящ и при совместном использовании возможно потенцированное отрицательное действие этих препаратов на организм человека. Необходим поиск новых методов лечения синовитов, который позволил бы уменьшить кратность внутрисустаного введения гормонов, побочные действия и осложнения которых при частом использовании хорошо известны и очевидны.
Акценты лечения
После проведения ЛСТ необходима комплексная терапия с использованием противовоспалительного препарата для пролонгации лечебного эффекта ЛСТ,что позволило бы уменьшить кратность повторных локальных стероидных инъекций, а в некоторых случаях и отказаться от них. Для увеличения продолжительности и усиления противовоспалительного эффекта ЛСТ,совместно с ЛСТ был использован отечественный противовоспалительный препарат артрофоон (АФ), содержащий в сверхмалых дозах (СМД) антитела к фактору некроза опухоли-α (ФНО-α), который по современным данным лежит в основе цитокинового каскада развития воспаления. Введение ингибиторов ФНО-α) в клиническую практику является одним из крупных достижений современной медицины [4]. Введение в организм СМД антител к эндогенным регуляторам физиологических функций (гормоны, цитокины, мембранные белки и др.)не блокирует функциональную активность молекул, к которым они выработаны, а модифицирует их эффекты.Антитела к эндогенным регуляторам физиологических функций в СМД специфически воздействуют на активность именно тех молекул, к которым они выработаны[7]. В частности, СМД антител к ФНО-α модифицируют активность именно ФНО-α и функционально сопряжен-ных с ним молекул, оказывая выраженное противовоспалительное и анальгетическое действие [8]. Ранее АФ неоднократно использовался как в виде монотерапии,так и в комплексном лечении ОА с хорошими клиническими результатами [1,3,9].
Материалы и методы лечения
Целью рандомизированного клинического исследования явилась оценка клинико-лабораторной эффективности терапии АФ больных остеоартрозом коленного сустава после однократной внутрисуставной инъекции 1 мл дипроспана, в сравнении с пациентами, у которых после однократной инъекции 1 мл дипроспана другаятерапия не проводилась.На базе поликлиники Центральной Клиническойбольницы (ЦКБ) было отобрано 40 больных ОА коленного сустава согласно критериям ACR, (Altman, R.et al., 1991)в стадии обострения с клинико-лабораторными призна-ками синовита. Всем больным синовит верифицировалсяс помощью ультразвукового исследования суставов.Критериями исключения из исследования являлись следующие.
1. Вторичный артроз коленного сустава включая: ревматоидный артрит, септический артрит, воспалительное заболевание сустава, подагру, псевдоподагру, болезнь Педжета, перелом сустава, акромегалию, фибромиалгию, болезнь Вильсона, охроноз, гемохроматоз, остеохондроматоз, наследственные заболевания суставов, повреждение менисков.
2. Нежелание прекратить физиолечение и прием препаратов, кроме исследуемых.
3. Любое тяжелое заболевание, требующее госпитализации на обследуемый период.
4. Беременные, кормящие матери или женщины детородного возраста, отказывающиеся использовать надежные методы контрацепции в течение всего периода исследования.
5. Пациенты с тяжелыми заболеваниями внутренних органов, требующие первостепенное лечение основного заболевания.
6. Пациенты, злоупотребляющие или имеющие зависимость от препаратов, кроме никотина.
Больные были разбиты по 20 человек на основную и контрольную группы. В основную группу вошли 5 мужчин,15 женщин, среднего возраста 63,5±8,7 лет и давностью заболевания 6,4±3,9 лет. I-я рентгенологическая стадия ОАпо Kellgren отмечена у 1-го больного, II-я – у 12 пациентов и III-я – у 7 больных. Контрольную группу составили 4 муж-чин, 16 женщин, среднего возраста 62,5±7,2 лет, и давностью болезни 5,7±2,8 лет. I-я рентгенологическая стадия ОАпо Kellgren выявлена у 2-х пациентов, II-я – у 11 больных и III-я – у 7 больных. Таким образом, основная и контрольная группы были сопоставимы по полу, возрасту, давности и стадии заболевания.Пациентам основной группы после однократной внутрисуставной инъекции 1 мл дипроспана с 10 мл 0,5%раствора новокаина с первого дня после инъекции была назначена монотерапия АФ в количестве 6 таблеток в сутки в течение 6 месяцев. Пациентам контрольной группы после однократной внутрисуставной инъекции 1 мл дипроспана с 10 мл 0,5% раствора новокаина в течение 6 меся-цев медикаментозная терапия ОА не проводилась.В обеих группах перед введением дипроспана с ново-каином при наличии значимого количества внутрисуставной жидкости проводилась ее максимальная аспирация.Пациентов, которым выполнялась аспирация, было 12 в основной группе и 11 в контрольной группе. Другая терапия больных ОА кроме рекомендаций по режиму При возникновении обострений в послеинъекционный период у больных обеих групп, после осмотра врача назначается диклофенак, принятый за «золотой стан-дарт» НПВП, в средней дозе 100 мг в сутки на период 7–10 дней. Врачом фиксировались количество больных из обеих групп и сроки начала приема НПВП после ЛСТ.При отсутствии эффекта от НПВП и сохранении обострения в виде синовита, проявлявшегося постоянной болью в суставе, припухлостью его, уменьшением подвижности сустава и/или наличием внутрисуставной жидкости при ультразвуковом исследовании, больному проводилась повторная инъекция дипроспана с новокаином в дозах,аналогичных 1-й инъекции, также с предварительным удалением жидкости из сустава. Таким образом, повторная инъекция дипроспана не выполнялась без предварительной попытки лечения обострения синовита НПВП. Сроки повторной инъекции после первой ЛСТ и количество пациентов, которым требовалась повторная внутрисуставная инъекция, также фиксировались врачом. Перед первой инъекций и в конце 6-го месяца проводился общеклинический осмотр пациентов обеих групп.Так же в данные сроки определялась выраженность боли в коленном суставе (по 100 миллиметровой визуальной аналоговой шкале – ВАШ), измерялась окружность коленного сустава на уровне середины надколенника в сантиметрах, измерялся объем движения в суставев угловых градусах, оценивалась функциональная недостаточность по опроснику WOMAC.По истечении 6 месяцев после инъекции у всех пациентов обеих групп оценивались показатели общего и биохимического анализов крови, общий анализ мочи.В начале и в конце лечения у больных оценивалась электрокардиограмма. При клинической констатации жидкости в суставе больным ОА выполнялось ультразвуковое исследование сустава в начале и в конце лечения. В процессе лечения анализировались побочные явления,а в конце терапии больной оценивал эффективность проведенного лечения.
Полученные результаты
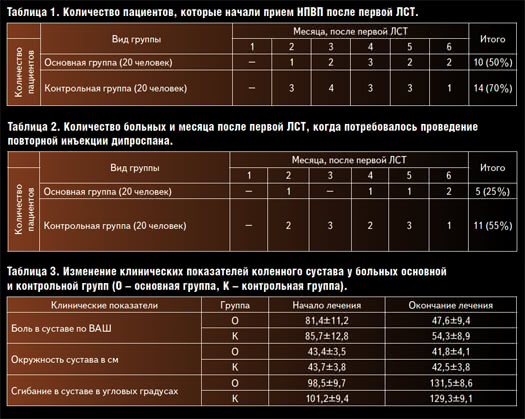
В первые дни после инъекции признаки клинического улучшения отмечены у большинства больных обеих групп и характеризовались уменьшением болей в суставе,уменьшением припухлости сустава, увеличением объема движений в нем, улучшением общего самочувствия. Больные отмечали улучшение местного процесса записями в индивидуальных картах наблюдения: «боль при ходьбе уменьшилась», «улучшилась походка», «перестала раскачиваться при ходьбе», «боль по вечерам ослабла», «уменьшились ночные боли», «поднялась на этаж без помощи лифта», «пришел в поликлинику без палочки», «стала испытывать радость от движения». У части пациентов уменьшилась раздражительность и нормализовался сон,прежде всего за счет уменьшения ночных болей.У пациентов основной группы, принимавших после ЛСТ АФ, уменьшение боли, припухлости сустава, увеличение объема движений в нем были более выраженными и длительными по срокам, чем у больных контрольной группы, не принимавших АФ. Пациенты, принимавшие АФ после ЛСТ, использовали НПВП в меньших количествах и в более отдаленные сроки, чем больные, не принимавшие АФ после ЛСТ. В таблице 1 представлены как сроки в месяцах после ЛСТ, когда пациенты начали прием НПВП,так и количество пациентов обеих групп, которые начали прием НПВП в определенный срок после ЛСТ.Из таблицы видно, что за 6-месячный период после ЛСТ,приемом НПВП воспользовалась только 10 пациентов из основной группы больных, принимавших АФ (50%), в то время как среди пациентов контрольной группы, не принимавших АФ после ЛСТ, число больных, которым потребовалось назначение НПВП, составило 14 человек (70%).Повторная инъекция дипроспана проводилась только при повторном обострении синовита после первой ЛСТ и при отсутствии эффекта от НПВП, назначенных на 10-дневный срок. В таблице 2 представлено количество пациентов и месяца после первой ЛСТ, когда потребовалось проведение повторной пункции сустава с введением дипроспана. Как видно из таблицы, необходимость в повторной инъекции дипроспана в основной группе,принимавшей АФ, возникала в более поздние срокии в меньшем числе случаев, чем в контрольной группе больных, не принимавших АФ. За 6-месячный период наблюдения после первой инъекции дипроспана повторная инъекция выполнялась 5 больным (25%) основной группы и 11 больным (55%) контрольной группы. При этом видно,что в контрольной группе больных повторные инъекции для купирования синовита проводились 5 пациентам из 10, принимавших НПВП на фоне АФ, что составило 50%. В контрольной группе, из 14 принимавших на фоне обострения синовита только НПВП, повторные инъекции дипроспана выполнялись 11 пациентам – 78,6%, что указывает на большую эффективность комплексной терапии синовитов НПВП в сочетании с АФ. За 6-месячный период наблюдения после первой ЛСТ, 3-я инъекция дипроспана не выполнялась ни одному больному.Таким образом, к концу 6-месячного наблюдения пос-ле первой инъекции дипроспана повторная инъекция не потребовалась 15 (75%) пациентам основной и 9 (45%)пациентам контрольной группы. У больных, которым повторные инъекции дипроспана с новокаином не выполнялись, оценивалось динамика клинических характеристик состояния коленного сустава: боль, припухлость, сгибание в угловых градусах, что представлено в таблице 3.Как видно из таблицы, после проведения однократной ЛСТ данные характеристики улучшились в обеих группах,но белее хорошие клинические результаты отмечены в основной группе, где пациенты после ЛСТ получали непрерывно на протяжении 6 месяцев АФ. Уменьшение болей и увеличение амплитуды движений в коленном суставе привели к положительной динамике индекса WOMAC. До лечения суммарный индекс WOMAC в основной группе составил 621,7±187,4 мм, а в конце лечения снизился до 381,7±161,8 мм. Индекс WOMACв контрольной группе пациентов, не принимавших АФ,уменьшился менее значительно – с 589,2±193,4 мм до 407,4±182,4 мм (рис. 1).
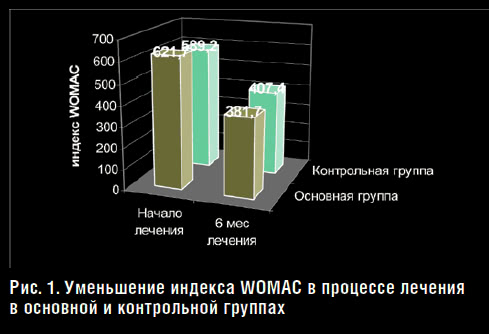
В обеих группа при лечении некоторые больные испытывали страх перед внутрисуставной инъекцией. В первые дни после ЛСТ часть больных обеих групп отмечала незначительное повышение АД, чувство«прилива», «жара» в голове, усиление аппетита. Часть больных обеих групп на фоне приема диклофенака отмечала тяжесть в животе, повышение АД. На фоне приема АФ в первую неделю у 1 пациента отмечался легкий кожный зуд, и гиперемия слизистых полости рта у другого пациента, прошедшие самостоятельно и не потребовавшие отмены АФ. Других побочных действий на фоне приема АФ не было. Из 20 больных основной группы, получавших АФ, результат лечения как очень эффективный отметили 3 пациента; как эффективную терапию данное лечение оценили 11 человек, без динамики оценили лечение 6 больных, а отрицательную динамику не отметил никто (рис. 2).
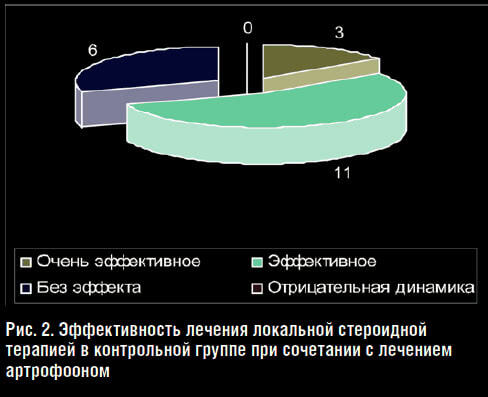
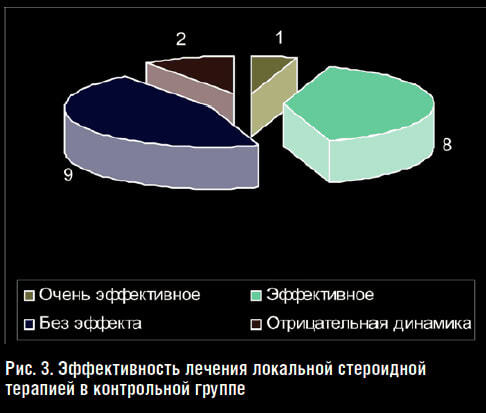
Из 20 больных контрольной группы результаты лечения как очень эффективные отметил 1 пациент; как эффективную – оценили 8 человек, без динамики ЛСТ оценили 9 больных, а как отрицательную – оценили 2 человека (рис. 3).
Показатели общего анализа и биохимических констант крови существенно не менялись в процессе лечения. Также не отмечено существенных изменений показателей общего анализа мочи. Значимых отклонений по ЭКГ, в процессе исследования, выявлено не было. Ультразвуковой контроль динамики количества внутрисуставной жидкости показал уменьшение ее количества после ЛСТ, а также явился ведущим методом для оценки показаний к повторной ЛСТ.
В целом можно отметить, что пациентам основной группы, получавшим АФ после ЛСТ, прием НПВП для купирования повторных обострений требовался реже в сравнении с пациентами контрольной группы. При этом, прием НПВП на фоне приема АФ оказывал более эффективное действие в купировании повторного синовита, что характеризовалось более редким проведением повторных внутрисуставных инъекций дипроспана как в целом, так и относительно больных,принимавших ПНВП в основной группе. Прием АФ после ЛСТ оказывал больший клинический эффект в сравнении с изолированной ЛСТ в виде более значительного уменьшения боли, уменьшения припухлости, увеличения подвижности в суставе, положительной динамики индекса WOMAC. Пациенты лучше оценивали лечениеЛСТ в сочетании с АФ по сравнению с изолированной ЛСТ. Результаты проведенного исследования позволяют констатировать хорошую переносимость АФ и его клиническую эффективность у больных ОА в сочетанной терапии с ЛСТ.
Таким образом, использование артрофоона в сочетании с ЛСТ больных остеоартрозом:
1) оказывает большую эффективность ЛСТ, что проявляется более выраженным уменьшением боли, припухлости, увеличением объема движений в суставе,положительной динамики индекса WOMAC в сравнениис обычной ЛСТ;
2) вызывает более выраженный и длительный лечебный эффект в сравнении с обычной ЛСТ, что проявляется сокращением повторных обострений синовитов;
3) позволяет сократить применение НПВП и уменьшить частоту повторных внутрисуставных инъекций глюкокортикостероидов;
4) хорошо переносится;
5) является терапией выбора, особенно при наличии противопоказаний к приему НПВП, особенно у пожилых людей, при патологии ЖКТ, повышении АД, застойной сердечной недостаточности, а также при неэффективности других методов лечения.
Литература
1. Алиханов Б.А. Опыт длительного применения сверх-малых доз антител к фактору некроза опухоли-и при ос-теоартрозе: эффективность и переносимость. Клиницист,2007.- № 4.- С. 63-672. Внутрисуставное и периартикулярное введениекортикостероидных препаратов при ревматических забо-леваниях. / А.Г. Беленький. М.: Российская мед. академияпоследипломного образования, 2001.- 63 с.3. Шостак Н.А, Павленко А.Ю., Хоменко В.В., КлименкоА.А., Бабадаева Н.А., Крутова Д.Ю. Исследование эффек-тивности и безопасности препарата артрофоон для леченияболевого синдрома у больных остеоартрозом коленногосустава. Вестник РГМУ, 2005.- № 8(47).- С. 45-484. Насонов Е.Л. Фармакотерапия ревматоидного артри-та с позиций медицины, основанной на доказательствах.Кремлевская медицина (клинический вестник), 2004.- №4.-С. 25-28.5. Ревматология: национальное руководство / под ред.Е.Л. Насонова, В.А. Насоновой.- М.: ГЭОТАР-Медиа, 2008.-С. 573-5896. Цурко В.В. Остеоартроз: проблема гериатрии.- М.:Изд. «Нью-диамед», 2004.- 136 с.7. Эпштейн О.И., Штарк М.Б., Дыгай А.М. и др. Фармако-логия сверхмалых доз антител к эндогенным регуляторамфункций. М.: Издательство РАМН, 2005.8. Козловская Л.В., Мухин Н.А., Рамеев В.В. и др. Потен-цированные антитела к фактору некроза опухоли-К. Бюлл.эксперим. биол. и мед. 2003; прил. 1: С. 68-71. 9. Черевкова Е.В. Клиническая фармакодинамикапрепарата Артрофоон, содержащего антитела к ФНО-,у больных с воспалительными заболеваниями суставов.Автореф. дис. … канд. мед. наук. Волгоград, 2005.10. American Academy of Orthopaedic Surgeons. AAOSclinical practice guideline on osteoarthritis of the knee.– Rosemont: American Academy of Orthopaedic Surgeons,2003. – 17 p.11. Arroll B., Goodyear_Smith F. Corticosteroid injectionsfor osteoarthritis of the knee: metaanalysis. B.M.J., 2004. – V.328 (7444). – P. 869.12. Creamer P. Intraarticular corticosteroid treatment inosteoarthritis. Curr. Opin. Rheum., 1999.- V. 11.- P. 417-421.13. Godwin M., Dawes M. Intraarticular steroid injections forpainful knees. Systematic review with metaanalysis. Can. Fam.Physician, 2004. – V. 50. – P. 24124–24128.14. Jordan K.M., Arden N.K., Doherty M. EULARRecommendations 2003: an evidence based approach to themanagement of knee osteoarthritis: Report of a Task Force of theStanding Committee for International Clinical Studies IncludingTherapeutic Trials (ESCISIT). Ann. Rheum. Dis., 2003. – V. 62.– P. 1145–1155.15. Pyne D., Ioannou Y., Mootoo R., Bhanji A. Intraarticularsteroids in knee osteoarthritis: a comparative study oftriamcinolone hexacetonide and methylprednisolone acetate.Clin. Rheumatol., 2004. – V. 23.- N 2. – P. 116–120.16. Raynauld J.P., Buckland-Wright C. Safety and efficacyof long-term intraarticular steroid injections in osteoarthritis ofthe knee: a randomized, double-blind, placebo-controlled trial.Arthritis Rheum, 2003.- V. 48.- P. 370-377.